Komunikat prasowy na temat analizy próbki szczepionki Synflorix seria ASPNB005AE
Do analizy tej próbki zastosowano metodę spektrometrii masowej do badania zanieczyszczeń w złożonych matrycach.
System ten jest szeroko stosowany w fazie badań i rozwoju szczepionek i okazał się bardzo pomocny w zastosowaniu do analizy składu produktu końcowego trafiającego na rynek.
Z analizy obrazowej pierwszego poziomu (badanie składu składników czynnych, zgodność z charakterystyką produktu leczniczego oraz zanieczyszczeń chemicznych i białkowych), wykryto że:
? antygeny nie zostały zidentyfikowane, tj. nie było możliwe ich sekwencjonowanie z powodu tworzenia się agregatów z aluminium, co czyniło je nierozpuszczalnymi i niestrawnymi.
Podobna charakterystyka została znaleziona w innych szczepionkach Glaxo (np.Infanrix hexa). Taka właściwość antygenów budzi wątpliwości co do bezpieczeństwa, ponieważ wiadomo, że adiuwant glinowy zawarty w szczepionce może być transportowany w mózgu przez specyficzne komórki układu odpornościowego, a zatem może również przenosić antygeny szczepionkowe z potencjalną neurotoksycznością.
Niezbędne jest sprawdzenie, czy agregaty glinu związane z antygenami szczepionkowymi są obecne w uszkodzonych tkankach mózgu.
? obecność dwóch zanieczyszczających białek w ilościach nie będących resztkami, tj. między nanogramami i mikrogramami, toksyczne zidentyfikowane w bazach danych:
? białko jądrowe EBNA-1, wykorzystywane do otrzymywania białek metodą rekombinacji DNA z wirusa Epsteina Barra (wirus powodujący mononukleozę oraz choroby nowotworowe)
? białko Acetylocholinoesteraza, enzym, który hydrolizuje ważny neuroprzekaźnik kwasu octowego i cholinę acetycoliny, pochodzenie tego zanieczyszczenia nie jest obecnie jasne.Fakt, że udało się zsekwencjonować i zidentyfikować te dwa białka potwierdza, że ??niestrawny i nierozpuszczalny agregat antygenów z glinem jest charakterystyczny dla tych antygenów, a nie jest błędem w metodzie analitycznej.
Skład i struktura molekularna tego agregatu zostaną dogłębnie zbadane.
Również obecność tych dwóch białek stwarza problem w zakresie bezpieczeństwa tej szczepionki, ponieważ oba mogą być potencjalnie toksyczne, jeśli dotrą do mózgu, co jest możliwe, jeśli zostaną przeniesione przez aluminium.
? obecność chemicznego zanieczyszczenia w ilościach nie będących pozostałościami, o wzorze chemicznym nadal nieznanym i nadal badanym.
Z tego pierwszego badania wynika, że ??szczepionkę można uznać za wadliwą, a zatem potencjalnie niebezpieczną dla zdrowia publicznego.
Aby móc zbadać związek przyczynowy z bardzo poważnym uszkodzeniem tkanek nerwowych, które doprowadziły do ??śmierci małego Szymona, konieczne jest kontynuowanie analizy szczepionki, mając na względzie badanie agregatu antygen- -aluminium, dwóch zanieczyszczonych białek zidentyfikowanych przez standardy kontroli, oraz nieznaną cząsteczkę chemiczną, te kwestie zostaną szczegółowo zbadane.
Kontynuujemy również analizę zanieczyszczenia materiałem genetycznym, w szczególności wirusa EBV i linii komórkowych wykorzystywanych do produkcji szczepionki.
Również w tym przypadku obecność zanieczyszczonego materiału genetycznego jest szczególnie niebezpieczna, jeśli jest przenoszona przez aluminium, ponieważ może powodować mutacje DNA i autoimmunizację, jak podano w literaturze dla innych szczepionek.
Zasadnicze znaczenie ma badanie tkanek zwłok ze specjalistycznymi metodami na wypadek powikłań poszczepiennych i dlatego należy zachować szczególną ostrożność podczas przeprowadzania sekcji zwłok i przechowywania próbek!
Dr Loretta Bolgan
RAPORT ZE WSTĘPNEJ ANALIZY
DANE OGÓLNE
| Dane klienta | OGOLNOPOLSKIE STOWARZYSZENIE WIEDZY O SZCZEPIENIACH STOP NOP |
|
Oznaczenie próbek |
Synflorix, seria:
– ASPNB201CA – ASPNB005AE |
| Otrzymano dnia | 26/03/2019 |
CEL ANALIZY
Kontrola składu produktu.
MATERIAŁY I METODY
4.8 – S.O.P. – Trawienie w cieczy za pomocą trypsyny V511A Promega (wersja 1.2 z dnia 04/09/2018)
4.5 – S.O.P. – Metoda MS: analiza trawiona tryptykiem (peptydy) (wer. 1.5 z dnia 30.10.2018)
4.1 – S.O.P. ? Metoda Bradforda oznaczania ilościowego białka (wer. 1.2 del 21/06/2018)
OTRZYMANE WYNIKI
Sprawdzenie zgodności produktu z informacjami zawartymi w charakterystyce produktu. LINK DO CHPL
| Składnik | Obecność | Związki jonowe |
| Polisacharyd pneumokokowy o serotypie 1 – 1 ?g | N.D. | |
| Polisacharyd pneumokokowy o serotypie 4 – 3 ?g | N.D. | |
| Polisacharyd pneumokokowy o serotypie 5 -1 ?g | N.D. | |
| Polisacharyd pneumokokowy o serotypie 6B – 1 ?g | N.D. | |
| Polisacharyd pneumokokowy o serotypie 7F – 1 ?g | N.D. | |
| Polisacharyd pneumokokowy o serotypie 9V – 1 ?g | N.D. | |
| Polisacharyd pneumokokowy o serotypie 14 – 1 ?g | N.D. | |
| Polisacharyd pneumokokowy o serotypie 18Cn – 3 ?g | N.D. | |
| Polisacharyd pneumokokowy o serotypie 19F – 3 ?g | N.D. | |
| Polisacharyd pneumokokowy o serotypie 23F – 1 ?g | N.D. | |
| Skoniugowany z białkiem nośnikowym D (pochodzącym z bezotoczkowych szczepów Haemophilus influenzae) 9?16 ?g | N.D. | |
| Skoniugowany z toksoidem tężcowym jako nośnikiem białkowym 5?10 ?g | N.D. | |
| Skoniugowany z toksoidem błoniczym jako nośnikiem białkowym 3?6 ?g | N.D. | |
| Chlorek sodu | N.D. | |
| Woda do wstrzykiwań | N.D. | |
| 2-fenoksyetanol | N.D. |
*N.D.: nie wykrywalne: poniżej granicy wykrycia technologii.
Analiza jakościowa (metoda Bradforda)
Na podstawie wbudowanej linii kalibracyjnej wykryto stężenie białka mniejsze niż 0,25 mg / ml.
Czyste Seria: ASPNB201CA Seria: ASPNB005AE
Frakcja białkowa
Wykryto sygnały potencjalnie związane z sekwencjami aminokwasowymi.
Po dalszej analizie zidentyfikowano możliwe dopasowania z białkami. Uzyskane wyniki są załączone z przetwarzaniem za pomocą MS-BLAST.
Załącznik ?1 – wyniki wyszukiwania BLASTP? odpowiada partii ASPNB201CA.
Załącznik ?2 – wyniki wyszukiwania BLASTP? odpowiadają partii ASPNB005AE.
Z przeglądu literatury dotyczącej białek zidentyfikowanych przez MS-BLAST wyłoniły się dwa białka potencjalnie szkodliwe dla ludzi (Tabela 1).
| Białko | Notatka naukowa |
| Białko jądrowe EBNA-1
[Rhodanobacter sp. Soil772] |
Wielofunkcyjne białko wirusowe, związane z dimerem.
Wirus Epsteina-Barra. |
| Acetylocholinoesterazy
[Streptosporangium roseum DSM 43021] |
Hydrolaza serynowa, która kończy działanie,
acetylocholina hydrolizuje ją w kwas octowy i cholinowy. |
Tabela 1
Poszukiwanie toksyn i zanieczyszeń.
Seria: ASPNB201CA
| Zidentyfikowany jon cząsteczkowy | Wzór podobny do struktury | Odpowiednie notatki naukowe |
| m/z = 237.2 | – | – |
Seria: ASPNB005AE
| Zidentyfikowany jon cząsteczkowy | Wzór podobny do struktury | Odpowiednie notatki naukowe |
| m/z = 237.2 | – | – |
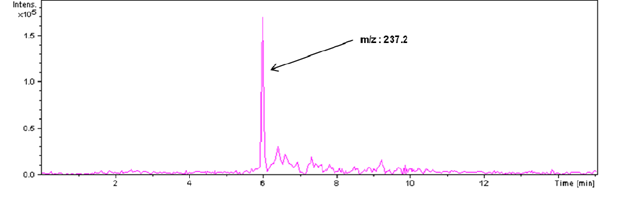
Jon o stosunku m/z 237,2 dał pik o wysokiej intensywności (fig. 1) w serii ASPNB005AE. W serii ASPNB201CA występuje obecność jonów, ale o mniejszej intensywności. Trwają dalsze badania umożliwiające ich identyfikację poprzez zaawansowane wyszukiwanie w bazach danych.
DODATKOWE UWAGI: Brak
Analizy są wykonywane przy użyciu technologii uznanej przez międzynarodową literaturę naukową (Albini A. i in
15.10.2015r.; 29 (19): 1703-10. doi: 10.1002 / rcm.7270; Rapid Commun Mass Spectrom.